逆转器官纤维化,MSC在行动!
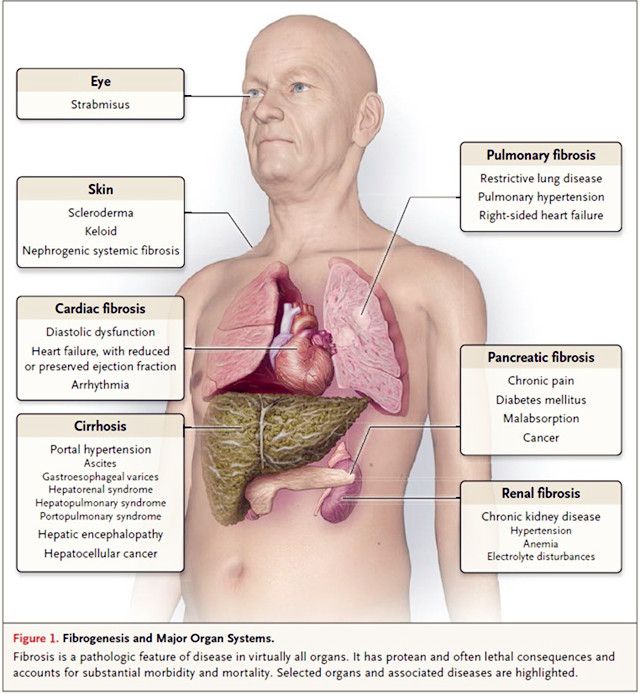
说起器官纤维化,可能离我们最近的就是疫情引起热论的“肺纤维化”,但其实,几乎在人体的各个器官都可能发生纤维化,主要常见的有肝纤维化、肺纤维化和肾纤维化。
——病毒、酒精等刺激因素攻击正常肝细胞使其损伤,且炎症细胞和肝星状细胞活化导致肝脏的正常结构和功能被破坏,最终发生肝纤维化。
——肺纤维化的发生与许多疾病相关,包括硬皮病(系统性硬化症)、结节病和感染,也可能是环境暴露(如矽尘或石棉)的结果,但大多数患者是特发性和累积进展的。肺纤维化主要表现为肺组织增厚或形成瘢痕、肺泡结构紊乱。
——肾纤维化是慢性肾病进展至终末期肾脏疾病的主要过程,伴随着高发病率和病死率,以肾小球硬化和肾小管间质纤维化为特征。
这些看似与炎症不相干的疾病其实都存在着慢性炎症微环境。正是这些慢性的炎症导致组织细胞不断受损,最终进展为不可逆病变。
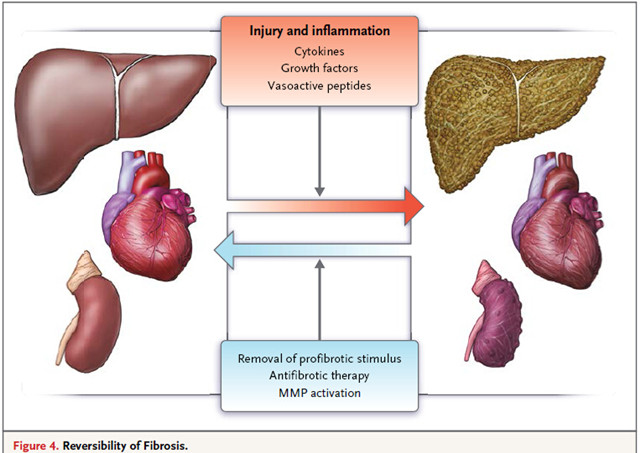
人体器官纤维化不可逆
纤维化和由此产生的器官功能衰竭至少占全世界死因的三分之一。因为纤维化较常见,对所有器官均可产生不良影响,所以它是治疗领域里一个有吸引力的目标。
器官纤维化是指由于人体内外复杂的工作机制和环境,器官在行使基本职能的过程中几乎不可避免的造成损伤,如果是较小的损伤,那么器官自身的实质细胞即可通过一系列修复措施将受损的器官恢复正常的结构和功能。然而,如果损伤较大,即损伤程度超过了实质细胞的修复能力时,细胞外基质就会大量增生以修复受损的组织,导致结缔组织异常增生,这时候就会发生器官的纤维化病理病变。
简单来说,纤维化疾病就是器官对于损伤的过度修复造成的。纤维化是由过量的结缔组织形成的,它会导致身体器官和皮肤出现瘢痕组织和遭受功能衰竭。随着纤维化程度的进一步加重,最终发展为器官硬化,乃至衰竭。
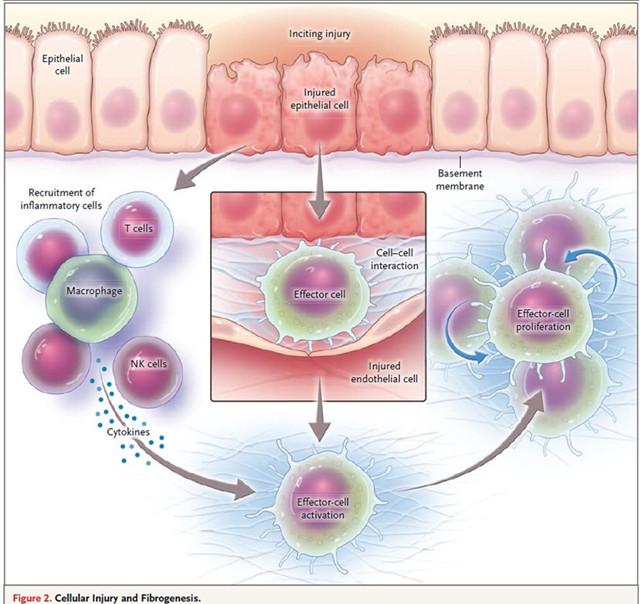
在一项新的研究中,来自杜克-新加坡国立大学医学院和新加坡国家心脏中心等研究机构的研究人员通过鉴定心脏、肾脏和其他组织中的慢性纤维化疾病的关键促进物,发现一种被称作白细胞介素11(IL11)的关键性蛋白导致纤维化疾病和器官损伤。相关研究结果于2017年11月13日在线发表在Nature期刊上,论文标题为“IL11 is a crucial determinant of cardiovascular fibrosis”。因此,这一突破性发现---抑制IL11能够阻止心脏和肾脏纤维化---有潜力改变对全世界数百万人的治疗方法。
MSC逆转器官纤维化
近年大量实验研究证明,纤维化是可以逆转的。有关组织纤维化分子细胞生物学的基础研究,特别是发现组织纤维化的发生发展是组织损伤后修复过度的结果,以及通过改变组织微环境可以改变组织纤维化程度的相关基础研究提示,组织纤维化进程是可以被改变的,组织纤维增生疾病是可以治疗的疾病。尽管仍然有不同意见,但都同意药物治疗可以分别逆转、消退和停滞组织纤维化病程。
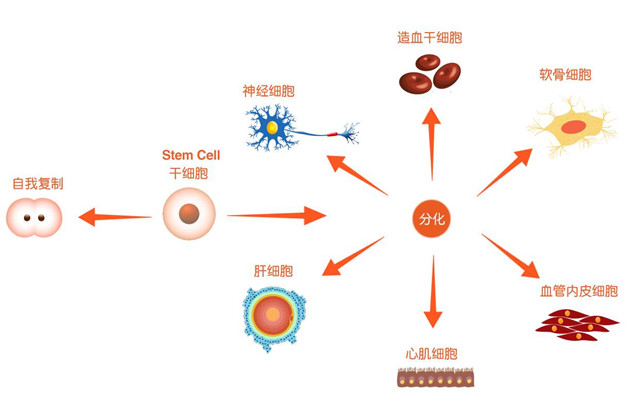
间充质干细胞(Mesenchymal stem cell, MSC)是一种多能干细胞,它具有干细胞的所有共性,即自我更新和多向分化能力。由于MSC来源广泛,获取培养、扩增、纯化也相对容易,免疫原性低,较少伦理冲突等优点,自1966年被首次发现以来,MSC 在组织工程、基因治疗和免疫治疗中的作用就备受瞩目,与其他干细胞或非干细胞相比,以MSC为基础的细胞治疗方式具有极大的优势。
MSC逆转纤维化机理
1、MSC具有“归巢”能力
MSC在体内能够按需迁移到靶组织器官后通过增值分化为受损的组织细胞进行器官修复。这种“归巢”现象是在受损器官分泌的生物因子的引导下完成的:MSC通过分泌的生长因子等细胞因子启动其它组织细胞的自我修复,如血管内皮细胞,组织干细胞等,MSC的这个作用称之为“细胞赋能”。生物因子充当“信使”引导MSC转移到受损伤的部位发挥作用。与药物治疗不同,植入体内的MSC在迁移、发挥作用后不会被代谢外排,而是与机体“合二为一”。
2、MSC多项诱导分化能力
既往的大量研究均显示了MSC具有极强的可塑性。在不同的细胞外微环境影响作用下,MSC可分化为各种来源于中胚层的细胞系,如脂肪细胞、成骨细胞、软骨细胞、肌细胞及心肌细胞等,同时还可分化为一些非中胚层的细胞,如干细胞和神经元。细胞水平的体外试验显示,MSC具有向肝细胞分化的潜能,分化所得的肝细胞同样具有合成白蛋白、尿素、储存糖原、摄取LDL及苯巴比妥诱导的细胞色素P450的表达等功能,与正常的肝细胞在形态及功能上具有高度的一致性。干细胞定向迁移到患病器官后,在器官特定的环境诱导下定向分化为和器官细胞相同的细胞,使得器官的实质细胞增多,提高器官运行能力,减轻纤维化程度。
3、MSC参与调节免疫反应、修复受损器官
在MSC移植治疗大鼠急性肝衰竭的研究中表明,干细胞分泌的IL-10是减轻大鼠肝损伤的重要炎症因子。MSC来到炎症部位后可以通过释放大量的抑制炎症的分子减轻局部的炎症反应,对局部的免疫微环境进行“负向”调控。研究人员还发现脂肪MSC分泌的肝细胞生长因子和血管内皮生长因子是促进干细胞增殖的关键因素,而分泌的巨噬细胞迁移抑制因子是抑制肝细胞纤维化的主要成分。除此之外,MSC分泌的相关酶类、干扰素都在复杂的治疗器官纤维化的过程中发挥作用。
近年来,MSC被广泛应用到了多种疾病的治疗研究中,日前,《干细胞转化医学》杂志上的最新研究显示,胎盘羊膜来源的MSC通过调节β细胞反应来抑制肺部炎症反应,从而阻止纤维化进展。研究指出,因此应鼓励这种MSC疗法的临床转化。

MSC逆转纤维化临床研究
早在2016年,国内专家就发表了MSC治疗肝纤维化的临床研究结果,他们将60例肝纤维变性引起的肝纤维化患者随机分为青霉胺组和MSC+青霉胺组,每组30例,记录治疗前后对肝纤维化,肝功能和血清学指标的治疗效果并进行比较。结果发现,治疗后两组的血清学指标水平均降低,而MSC+青霉胺组的细胞因子水平明显低于青霉胺组。说明MSC和青霉胺的联合治疗对肝豆状核变性引起的肝纤维化具有明显的积极作用。
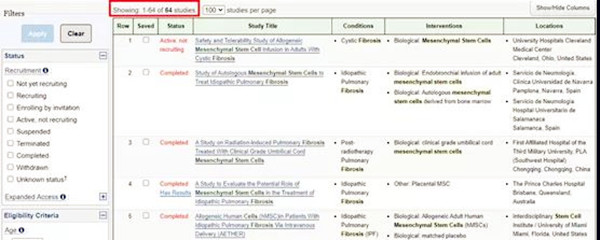
2017年,期刊《Chest》在线发表了一项关于同种异体人MSC治疗特发性肺纤维化I期安全性临床试验。9例轻度至中度特发性肺纤维化患者分成三组,静脉输注不同浓度的MSC。60周后的评估结果表明未发生严重不良事件,证明了MSC输注治疗轻、中度特发性肺纤维化的安全性。
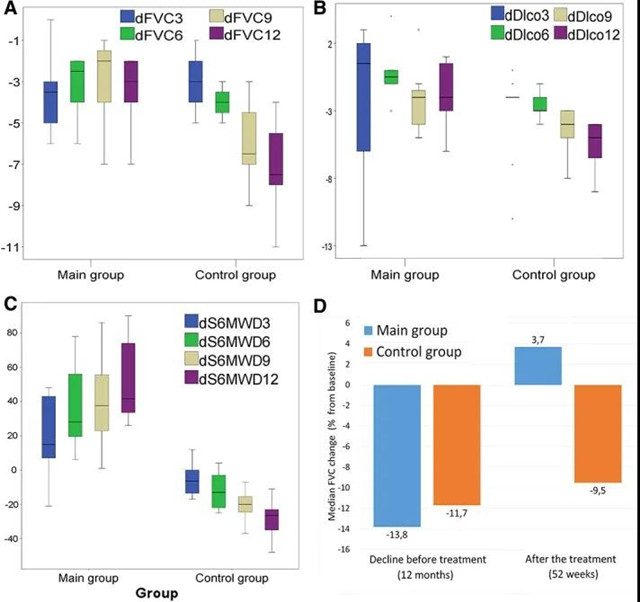
2019年,《干细胞转化医学》杂志报道了人体内高剂量MSC治疗特发性肺纤维化伴肺功能快速下降的临床研究结果。20名受试者被随机分为两组,分别为MSC治疗组和安慰剂组。肺功能指标的分析显示,MSC具有一定的治疗效果,遏制了肺纤维化的快速发展,安全性评估未发现治疗相关的显著不良反应事件,证明了MSC治疗的有效性和安全性。
展 望
MSC疗法为纤维化疾病的临床治疗提供了新思路,通过协调,从结构和功能上修复或再生纤维化的组织器官,使其发挥正常的生理功能。但是目前相关治疗的临床试验还存在样本量较少等问题,对更详细的作用机制的了解也不够深入。随着大量临床研究的开展,相信纤维化疾病的干细胞疗法将更加成熟,安全应用MSC治疗疾病不再是奢望。
生命初始,弥足珍贵。宝宝出生时,是获取最高质量/高纯度的干细胞机会。从爱与亲情链接的“脐带”获得的MSC拥有新生细胞强劲的生命力,含有自身干细胞的精华部分,能更快激活休眠细胞,促进细胞自我修复更新,恢复器官组织和生理功能,对人体健康和延缓衰老都大有裨益。干细胞的存储和治疗是未来医学的发展方向,早一天存储,早一天受益。
